Aufgrund der vielen durchgeführten Studien lässt sich sagen, dass das Glaukom wahrscheinlich PRIMÄR EINE VASKULÄRE KRANKHEIT mit anfänglicher, durch einen Durchblutungsmangel bedingten Schädigung des Sehnervenkopfes und der Lamina cribrosa ist. Während der intraokuläre Druck (IOD) sicherlich ein Risikofaktor ist, hat das Fortschreiten des Glaukoms vermutlich mehr mit der Ischämie durch einen verringerten Augenperfusionsdruck (APD) / okulären Perfusionsdruck (OPP, engl. ocular perfusion pressure) zu tun, angesichts dessen, dass das Fortschreiten bei jeder Art von IOD stattfindet. Forschungsergebnisse der letzten Jahrzehnte liefern triftige Beweise dafür, dass die Glaukom-Progredienz aufgrund eines reduzierten Blutstromes zum Auge erfolgt, insbesondere am Sehnervenkopf, wenn kompensatorische alternative Blutzufuhren die Funktion einstellen. Es besteht aber auch kein Zweifel, dass ein erhöhter oder instabiler IOD die Situation der verringerten Blutzufuhr verschärft oder dazu beiträgt und die daraufhin erfolgenden ischämischen Schädigungen einen Teufelskreis erzeugen, der weitere Schäden und einen fortschreitenden Sehverlust einleiten.
Das Glaukom ist die zweithäufigste Ursache für das Erblinden, an zweiter Stelle hinter Katarakten, und steht weltweit an erster Stelle beim Ursprung irreversibler Blindheit. Geschätzt sind 60 Millionen Menschen derzeit davon betroffen. Die am meisten diskutierte Form des Glaukoms ist das primäre Offenwinkel-Glaukom. Es gibt jedoch viele Subtypen des Glaukoms, die jeweils durch spezifische Gesichtsfeldausfälle, Defekte der retinalen Ganglienzellen (RGC) und retinalen Nervenfaserlagen (RNFL) und vor allem die Exkavation (Vertiefung) am Sehnervenkopf charakterisiert sind. Von einem primären Glaukom spricht man in Fällen, in denen der IOD ohne ersichtlichen Grund erhöht ist, während man den Begriff sekundäres Glaukom verwendet, wenn eine zugrundeliegende Ursache für den erhöhten IOD entdeckt wird. Demgegenüber wird ein Glaukom bei Fällen mit normalem IOD als Normaldruckglaukom (NTG) bezeichnet. Der Begriff Glaukom wird üblicherweise als Sammelbegriff für eine Reihe von Augenerkrankungen betrachtet, denen unterschiedliche pathophysiologische Prozesse zugrunde liegen und die eine starke Exkavation des Sehnervenkopfes (ONH) zur Folge haben.
Das auch als glaukomatöse Optikusneuropathie (GON) bezeichnete Glaukom ist gekennzeichnet durch eine durch RGC-Axonen-Verlust bedingte Exkavation am Sehnervenkopf. GON ist die einzige Optikusneuropathie, von der man weiß, dass sie dieses auffällige „ausgehöhlte“ oder „exkavierte“ Erscheinungsbild des Sehnervenkopfes erzeugt.
Früher hielt man den erhöhten IOD für die Ursache des Glaukoms, insbesondere da eine Senkung des IOD nachweislich das Fortschreiten des Glaukoms abschwächt. Man nahm an, dass dieser erhöhte IOD den ONH durch mechanischen Stress beschädigt. Diese Theorie konnte jedoch nicht erklären, wieso der überwiegende Teil der Menschen mit hohem IOD (d.h. okularer Hypertension) niemals ein Glaukom entwickeln und weshalb viele Patienten mit normalem oder niedrigem IOD weiterhin einen Sehverlust aufgrund eines fortschreitenden Glaukoms erleiden. Tatsächlich ist es so, dass die Forschung deutlich zeigt, dass ein Glaukom sich bilden und weiter ausbilden kann, ohne dass IOD vorliegt. Diese anscheinend paradoxen Datensätze deuten auf einen weiteren Mechanismus bei der Entstehung eines Glaukoms hin, bei dem die Schädigung wahrscheinlich eher vaskulären als mechanischen Ursprungs ist.

Die Definition des Glaukoms entwickelt sich langsam weiter, da das Glaukom nun als primäre Optikusneuropathie angesehen wird, und nicht als Folgeerkrankung eines hohen IOD. Diese neue Definition wird nicht von allen Fachkräften im Gesundheitswesen angenommen oder zu Bildungszwecken vor der Allgemeinheit verwendet, da obsolete Phrasen, die das Glaukom als eine Erkrankung des „hohen Augeninnendrucks“ beschreiben, im Bereich der Patientenversorgung noch immer in Verwendung sind. Die Patienten, und sogar manche Dienstleister im Bereich der Augenheilkunde, beschreiben sogar die IOD-Messungen als den „Glaukom-Test“. Vielleicht verwenden die Augenärzte diese überholten Begriffe aus Gewohnheit, weil sie den Patienten geläufig sind, oder aus dem Versuch heraus, das medikamentöse Einnahmeverhalten der Glaukom-Patienten zu verbessern. Erschwerend kommt hinzu, dass grundsätzlich alle Glaukom-Therapien nur die Senkung des IOD zum Ziel haben. Obwohl das Glaukom offensichtlich nicht durch zu hohen IOD verursacht wird, betonen die Behandlungsstrategien und die Patienteninformationen ständig die Rolle des IOD als Übeltäter.
Leider ist diese zu stark vereinfachte Terminologie und Argumentation leicht zu begreifen und findet weite Verbreitung – aber sie ist dennoch ungenau und überholt.
Der IOD bleibt jener Faktor, der sich am leichtesten modifizieren lässt, und das ist zum Teil auch der Grund, weshalb Glaukomtherapien sich auf die Senkung des Augeninnendrucks konzentrieren. Die Forschung zeigt unbestreitbar, dass ein hoher IOD das Risiko, an Glaukom zu erkranken, erhöht. Ebenso wird durch die Senkung des IOD bei NTG das Risiko des Fortschreitens verringert.
Selbst wenn man alle anderen Variablen berücksichtigt, steigt die Prävalenz des Glaukoms mit dem Alter.
Im Allgemeinen tritt das Glaukom häufiger bei Menschen afrikanischer oder hispanischer Abstammung auf, während manche Arten von sekundärem Glaukom bei den asiatischen Völkern weit verbreitet sind. Kaukasische Populationen weisen eine niedrigere Häufigkeit bei Glaukom auf.
Studien lassen darauf schließen, dass eine starke Kurzsichtigkeit einen Glaukom-Risikofaktor darstellt, möglichweise aufgrund dünnerer okularer Strukturen, insbesondere einer dünneren Lamina cribrosa, die mehr gedehnt und weniger vaskularisiert werden.
Eine geringe zentrale Hornhautdicke ist ein Risikofaktor, möglicherweise aus denselben Gründen wie bei starker Kurzsichtigkeit, weil eine dünne Hornhaut oftmals von einer dünnen Lamina cribrosa begleitet wird. Zusätzlich können dünne Hornhäute fehlerhafte IOD-Messungen verursachen, sodass anstatt des tatsächliche IOD künstlich niedrigere Werte angezeigt werden.
Ein Verwandter ersten Grades mit Glaukom erhöht das Risiko, an Glaukom zu erkranken, vor allem bei Geschwistern. Obwohl mehrere Gene mit dem Glaukom assoziiert werden, wird angenommen, dass diese Krankheit polygen und stark von der Umwelt beeinflusst ist.
Ein Glaukom tritt häufig bei Personen mit Diabetes oder Bluthochdruck auf, obwohl manche Forscher skeptisch sind, was den Zusammenhang betrifft. Beide Erkrankungen verursachen eine vaskuläre Dysregulation, die die Blutzufuhr zum ONH stören kann. Beim Diabetes entsteht ein vaskulärer Insult durch die Beschädigung des Endothels der Blutgefäße, mit der möglichen Felge einer vaskulären Dysregulation. Bluthochdruck (Hypertension) verursacht einen Gefäßwiderstand, der zu einer GON führen kann. Umgekehrt kann ein übermäßig niedriger Blutdruck (Hypotension) den APD des ONH sogar senken, was bei antihypertensiven (d.h. blutdrucksenkenden) Medikamenten beachtet werden muss. Eine aggressive Senkung des Blutdrucks bei Patienten mit Bluthochdruck kann den Patienten anfällig machen für eine GON. Zusätzlich wird angenommen, dass eine durch eine Schlafapnoe verursachte Hypoxie (Sauerstoffmangel) das Risiko für die Entstehung und das Fortschreiten eines Glaukoms fördert.
Ein paar erste Studien lassen vermuten, dass ein gesunder Ernährungsstil und regelmäßige Bewegung dem Sehverlust nach einer Glaukom-Diagnose vorbeugen können. Zum gegenwärtigen Zeitpunkt sind solche Studien noch nicht beweiskräftig. Sollten systemische Vaskulopathien einen Patienten jedoch für ein Glaukom prädisponieren, dann ist es plausibel, dass ein gesunder Lebensstil die vaskuläre Dysregulation verringern und damit das Glaukom-Risiko reduzieren könnte.
Die Glaukom-Diagnose wird bei einer Routineuntersuchung mittels Opthalmoskopie (Augenspiegelung; visuelle Evaluierung des Sehnervs), Perimetrie (Messung des peripheren Gesichtsfeldes) und optischer Kohärenztomographie (moderne Scans, die die Dicke der RNFL und RGC-Lagen messen und so die Schwere des Glaukoms erkennen lassen) gestellt.
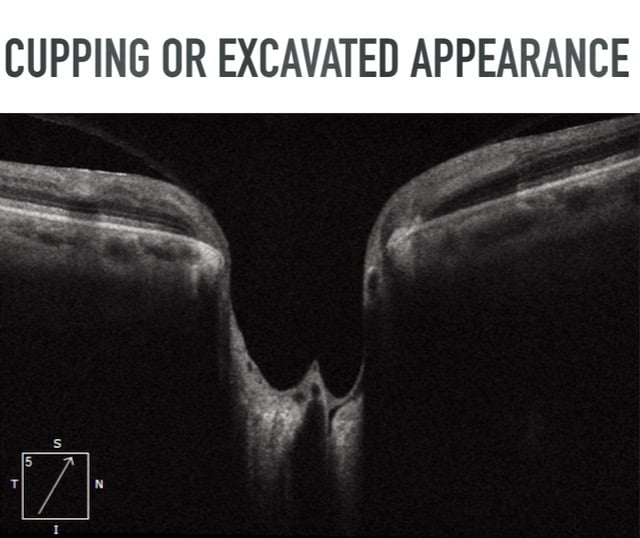
Die stereoskope Opthalmoskopie zeigt einen ONH mit einer „Exkavation“, d.h. einer „Aushöhlung“, dort, wo die Axone der RGC abgestorben sind, in der Nähe der peripapillaren Netzhaut, der Sehnervenscheibe oder der Lamina cribrosa. Diese Exkavation (engl. cupping) oder Vertiefung findet sich selten beim ONH und wird als äußerst pathognomonisch für eine Glaukom betrachtet. Bei einer klinischen Untersuchung können sich dann eine fokale Verdünnung des Sehnervenrandes, ein vertikal verlängerter CDR-Wert (engl. cup-disc-ratio), geknickte Blutgefäße, eine peripapilläre Atrophie oder Hämorrhagien der Sehnervenscheibe zeigen. Die Perimetrie stellt Gesichtsfeldstörungen dar, die mit Schädigungen des Nervenfaserbündels zusammenhängen, wie etwa einen nasalen Sprung, ein Bogenskotom, halbseitige Gesichtsfeldausfälle oder generalisierte Störungen, die häufig bei einem fortgeschrittenen Glaukom auftreten.
Erstmanifestation des Glaukoms: Eine der Herausforderungen bei der Diagnose und Behandlung des Glaukoms ist, dass die Erkrankung anfangs asymptomatisch verläuft. Die Patienten bemerken die Symptome normalerweise erst, wenn die Erkrankung bereits im fortgeschrittenen Stadium ist. Erkrankungen wie das Glaukom, bei denen die Symptome nicht zu der Schwere der strukturellen Veränderungen passen, gelten als strukturell-funktional dissoziiert. Mindestens 30-40% des Nervengewebes müssen beschädigt sein, bevor eine solche strukturale Anomalie zu funktionalen Symptomen oder Sehverlust führen. Das fehlen okularer Symptome am Anfang (insbesondere, wenn die Krankheit langsam voranschreitet), scheinen von der Plastizität des Gehirns maskiert zu werden, da das Gehirn die verringerte visuelle Signalübertragung kompensiert. Eine weitere Erklärung, die vorgeschlagen wurde, ist das Phänomen des Zur-Gewohnheit-Werdens („Habituation“) der langsamen Verschlechterung des Sehvermögens über einen langen Zeitraum hinweg nach Entstehung und Fortschreiten der Erkrankung. Das ist wahrscheinlich der Grund, weshalb die an einem Glaukom Leidenden sich selten über einen Sehverlust beschweren oder ein solches Nachlassen der Sehkraft nicht als „visuell bedrohliche Symptome“ betrachten.
Dennoch können in diesem Stadium einige Veränderungen des Sehvermögens oder Anzeichen für eine Verschlechterung der Sehkraft offensichtlich sein, auch wenn das selten der Fall ist. Zu den unbemerkten Symptomen des Glaukoms in diesem Stadium zählen eine erhöhte Lichtempfindlichkeit, schlechteres Nachtsehen und eine schwaches bis moderates „Schatten-“ oder „Nebelsehen“.
Glaukom im fortgeschrittenen Stadium: Im fortgeschrittenen Stadium der GON machen sich dann Symptome eines eingeschränkten peripheren Gesichtsfeldes, die oft zu Schwierigkeiten beim Navigieren in Räumen und zwischen Gegenständen führen, bei den Patienten bemerkbar. Die Patienten erwähnen mitunter, dass sie beim Gehen gegen die Wand laufen oder mit Gegenständen zusammenstoßen. Zu diesem Zeitpunkt tauchen spezifische Symptome auf wie das „Nebelsehen“, eine starke Blendung und ein stark verringertes Sehvermögen in einem schwach beleuchteten Umfeld. Bei einer ersten ophthalmologischen Untersuchung führen solche Symptome sofort dazu, dass ein Glaukom auf die differenzialdiagnostische Abklärungsliste gesetzt wird. Tragischerweise führt das Glaukom im Endstadium auch zu einem Ausfall des zentralen Gesichtsfeldes oder sogar zu völligem Erblinden.
Das Glaukom wird normalerweise bei einer routinemäßigen Augenuntersuchung diagnostiziert oder bei einer Augenuntersuchung, die aus einem spezifischen Grund durchgeführt wird (wie etwa einer jährlichen Diabetes-Augenuntersuchung), zufällig entdeckt. Der Patient zeigt zum Zeitpunkt der Diagnose fast nie Symptome. Da das Glaukom fast immer asymptomatisch verläuft, tun sich die Patienten schwer damit, die Anweisungen ihrer medizinischen Behandlung zu befolgen, denn es zeigen sich keine Symptome, die die Patienten daran erinnern, dass ihnen ein Sehverlust potenziell bevorsteht.
Ungefähr 3-6 Millionen Amerikaner und 4-7% der Menschen im Alter von über 40 Jahren haben einen erhöhten IOD ohne Anzeichen für einen glaukomatösen Sehnervenschaden. Der Normalwert für den IOD beträgt 10-21 mmHg, der Durchschnittswert ist 16 mmHg. Daher wird bei einem Wert von über 21 das Auge als okulär hypertensiv klassifiziert. Dieser erhöhte Druck kann das Resultat einer verringerten Wasserableitung, vermehrter Wasserproduktion, oder aber es könnte der normale Wert für das Auge sein, denn der IOD wird auf einer Gaußkurve (Glockenkurve) gemessen. Patienten mit erhöhtem Augeninnendruck (OHTN) verspüren keinen Druck und sehen nicht verschwommen. Beim OHNT kommt es zu keiner Exkavation der Sehnervenscheibe, Gesichtsfeldausfällen, Verdünnung der RNFL oder dem Verlust von RGC, denn das würde bedeuten, es handelt sich um ein Glaukom, nicht OHTN. Daher spricht man bei Patienten mit hohem IOD, die keine glaukomatösen Schäden aufweisen, von Patienten mit OHTN oder Glaukom-Verdachtsfällen.
Da kein etablierter Pflegestandard für OHTN-Patienten existierte, wurde die Ocular Hypertension Treatment Study (OHTS) entwickelt, um die Effizienz und den Nutzen zu bewerten, den das Einleiten einer IOD-senkenden Behandlung für das Hinauszögern oder die Vorbeugung eines Glaukoms haben kann. Die OHTS stellte fest, dass nach 5 Jahren die kumulative Wahrscheinlichkeit, ein Glaukom zu entwickeln, bei Patienten, die IOD-senkende Medikamente einnahmen, nur 4,4% betrug. Im Unterschied dazu lag der Wert für die unbehandelte Kontrollgruppe bei 9,5%. Die Ergebnisse der OHTS sollen jedoch nicht andeuten, dass alle Patienten mit erhöhtem IOD mit augeninnendrucksenkenden Medikamenten behandelt werden sollen, und die Forscher geben zu, dass eine längerfristige und unbegrenzte Medikation Nachteile aufweisen kann, insbesondere was die finanzielle Belastung und die Auswirkung auf die Lebensqualität betrifft. Wichtig ist, dass diese Studie auch Risikofaktoren für das Entstehen eines Glaukoms identifiziert hat, nämlich jene, die zuvor erwähnt wurden.

Auffallend ist vor allem, dass NUR 9,5% der unbehandelten OHTN-Patienten innerhalb von 5 Jahren ein Glaukom entwickelten. Die OHTS identifizierte relevante Risikofaktoren, welche die Wahrscheinlichkeit erhöhen, dass OHTN-Patienten letztendlich ein Glaukom ausbilden. Aus den Ergebnissen der OHTS und ähnlichen Studien lässt sich schließen, dass das alleinige Auftreten einer okuläre Hypertension nicht zwingend oder ausreichend ist, um die Ausbildung eines Glaukoms zu verursachen. Zudem besteht bei OHTM-Patienten eine Wahrscheinlichkeit von weniger als 10%, dass sie innerhalb von 5 Jahren ein Glaukom entwickeln werden. Anders ausgedrückt: Mehr als 90% der unbehandelten OHTN-Patienten werden innerhalb von 5 Jahren kein Glaukom entwickeln. Ergebnisse wie diese zeigen deutlich, dass ein hoher IOD das Risiko für die Entstehung und das Fortschreiten eines Glaukoms zwar erhöht, ein hoher IOD alleine aber noch nicht ausreicht, um eine Behandlung mit Medikamenten gegen die okuläre Hypertension zu rechtfertigen. Hinzu kommt, dass 4,4% der OHNT-Patienten, die erfolgreich mit IOD-senkenden Medikamenten behandelt wurden, TROTZDEM innerhalb von 5 Jahren ein Glaukom entwickelten. Außerdem demonstriert die Mehrheit der großen Glaukom-Studien (Advanced Glaucoma Intervention Study, Collaborative Normal Tension Glaucoma Study, Collaborative Initial Glaucoma Treatment Study, Early Manifest Glaucoma Trial)
ein Fortschreiten des Glaukoms trotz eines signifikant gesenkten IOD. Diese weithin anerkannten Resultate deuten an, dass das Glaukom viel komplizierter und vielschichtiger ist, als nur in Zusammenhang zu stehen mit einem erhöhten oder fluktuierenden IOD.
Augenärzte evaluieren die Progression des Glaukoms auf Basis der strukturalen und funktionalen Metriken. Strukturale Messungen werden mithilfe der Technologie der optischen Kohärenztomographie (OCT) gewonnen, bei der die Dicke der Axonen im Umkreis des ONH ermittelt wird. Eine Software für die Guided Progression Analysis (GPA) analysiert die Daten auf lange Sicht, um die Änderungsrate zu quantifizieren, und zeichnet die Ergebnisse in einer Kurve auf. Dieses Diagramm stellt den gegenwärtigen Grad des Fortschreitens dar und liefert auch eine Prognose für das weitere Fortschreiten in der Zukunft. Die funktionale Progression wird bedingt durch den Gesichtsfeldausfall, der mittels automatisierter Perimetrie geschätzt und mit früheren Werten verglichen wird. Diese Datensätze zeigen an, ob eine Progression „möglich“, „wahrscheinlich“ oder „bestätigt“ ist.
Wurde die Progression bestätigt, so wird ein „Ziel-IOD“ unter Zuhilfenahme des gegenwärtigen IOD, dem Prozentsatz der erwünschten IOD-Reduktion und dem Grad des strukturalen und funktionalen Ausfalls ermittelt. Da die medikamentösen und chirurgischen Behandlungsmethoden bei Glaukom sich gegenwärtig nur auf das Senken des IOD konzentrieren, wird ein „Ziel-IOD“ für den jeweiligen Patienten individuell ermittelt. Obwohl Studien validieren, dass das Senken des IOD den Grad des Fortschreitens des Glaukoms reduziert, haben diese Studien auch bestätigt, dass Glaukome oft fortschreiten, obwohl dieser „Ziel-IOD“ erreicht worden ist. Eine solche Beweislage deutet an, dass noch andere Faktoren als nur der IOD zum Fortschreiten eines Glaukoms beitragen.
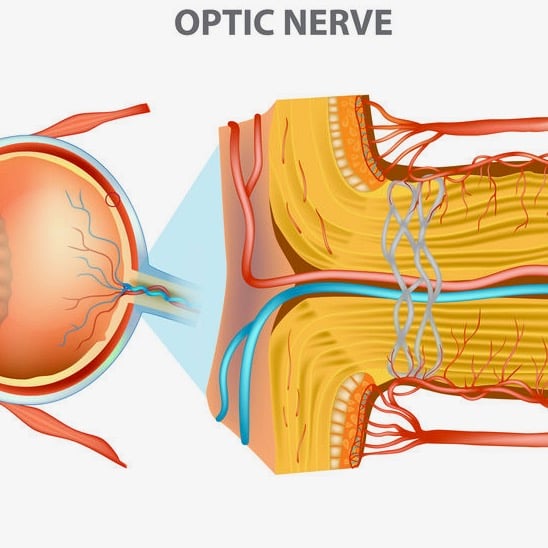
Während ein erhöhter IOD als Risikofaktor für das Fortschreiten der Erkrankung als allgemein anerkannt gilt, ist ein niedriger okulärer Blutfluss oder okulärer Perfusionsdruck (OPP; Augenperfusionsdruck, APD) vielleicht ein noch viel signifikanterer Risikofaktor. Der OPP/APD wird definiert als der Unterschied zwischen dem arteriellen Blutdruck und dem IOD. Daher senken sowohl ein hoher IOD als auch ein niedriger BD den OPP und initiieren ischämische Schäden an der Netzhaut und dem Sehnerv. Die Forschung zeigt, dass Patienten mit niedrigem OPP ein beträchtlich höheres Risiko für ein Fortschreiten des Glaukoms besitzen, wenn man sie in Vergleich setzt zu Patienten mit hohem OPP. Zudem steht die Progredienz in Zusammenhang mit OPP-Fluktuationen bei inkonsistentem BD oder IOD. Der Blutdruck ist in der Nacht aufgrund von tageszyklischen Mustern für gewöhnlich niedriger, Studien haben jedoch bestätigt, dass der progrediente glaukomatöse Gesichtsfeldausfall bei einem übermäßigen nächtlichen Blutdruckabfall auftritt.
Die Thessaloniki Eye Study wies eine starke Exkavation und einen schrumpfenden ONH-Randbereich bei nicht glaumatösen Patienten nach, die blutdrucksenkende Medikamente zu sich nehmen und deren diastolischer BD über Nacht unter 90 mmHg sank. Ebenso wurde zwischen einem Blutdruckabfall von 10% oder mehr bei Glaukoma-Patienten mit gut eingestelltem Bluthochdruck ein Zusammenhang mit einer strukturalen ONH-Schädigung und fortschreitendem Gesichtsfeldausfall festgestellt. Zudem korreliert die Größenordnung der OPP-Fluktuationen mit der Schwere des Glaukoms bei NTG-Patienten.
Neue bildgebende Verfahren zur Darstellung der Gefäße zeigen einen verringerten okulären Blutfluss (OBF) bei Glaukom-Patienten, insbesondere in Fällen, in denen das Glaukom trotz normalem IOD fortschreitet. Zudem kann das Fortschreiten der Glaukomentwicklung anhand der verminderten OBF-Rate sogar vorhergesagt werden. Fluktuationen des okularen Blutflusses sind besonders schädlich und mögen ein signifikanteres Maß für das Fortschreiten sein, als die OBF-Messwerte zu Behandlungsbeginn.
Die intrinsische Fähigkeit der vaskulären Autoregeneration dient der kontinuierlichen Bereitstellung von Sauerstoff und Nährstoffen trotz Irregularitäten bei Metabolismus oder Druck. Die Bedeutung der Autoregulation liegt in der Fähigkeit des Körpers, einen konstanten okularen Blutfluss (OBF) trotz eines inkonsistenten okularen Perfusionsdrucks (OPP) aufrecht zu erhalten. Die autoregulatorische Reaktion verändert den OBF in Reaktion auf Veränderungen des OPP. Obwohl ein erhöhter IOD zu einem verringerten OPP führt, ermöglicht die normale Autoregulation eine mikrovaskuläre Konsistenz, wodurch ein ischämischer Schaden verhindert wird. Der ONH wird jedoch empfindlich für OPP-Fluktuationen, wenn die Autoregulation gefährdet ist oder ihre regulatorische Bandbreite überschritten wird. Eine solche Autoregulationsbeeinträchtigung ist ein potenzieller vaskulopathischer Mechanismus für das Entstehen des Risikos eines fortschreitenden GON trotz relativ normaler IOD- und BD-Fluktuationen. Obwohl der OPP sich aufgrund eines hohen IOD oder niedrigen BD senken kann, hat die Forschung noch nicht deutlich gezeigt, welcher Fall, wenn überhaupt, dem ONH mehr schadet. Untersuchungen lassen jedoch vermuten, dass dieses Autoregulationssystem einen durch einen hohen IOD hervorgerufenen niedrigen OPP besser reguliert als einen durch einen durch einen niedrigen choroidalen BD hervorgerufenen, was darauf hindeutet, dass ein niedriger Blutdruck bei GON eine signifikantere Rolle spielt als ein hoher IOD. Auch haben Studien bei Glaukom-Patienten mit sowohl normalem als auch erhöhtem IOD einen niedrigeren BD und eine größere nächtliche Variation nachgewiesen.
Während die Blutzufuhr zum ONH durch die parapapilläre Aderhaut sich normalerweise autoregulieren kann, um einen konstanten OPP aufrecht zu erhalten, können signifikante Veränderungen bei BD und IOD diese Autoregulationsfähigkeit übersteigen. Wenn entweder die Bandbreite der Autoregulation überschritten oder die Autoregulationsfunktion beeinträchtigt ist, besteht die Gefahr der ischämischen Schädigung des ONH. Studien deuten auch auf eine Dysregulation oder sogar Nicht-Regulation der okularen Vaskulatur bei Glaukom-Patienten hin. Eine solche Dysregulation oder Nicht-Regulation birgt eine erhebliche Gefahr für den ONH bei normalen BD- und IOD-Fluktuationen, geschweige denn bei abnormalen Fluktuationen. Zudem kann es sein, dass der Verlust der Autoregulationsfunktion den ONH zusätzlich für GON prädisponiert, wenn er einem hohen IOD oder niedrigem BD ausgesetzt ist.
Some researchers believe systemic primary vascular dysregulation (PVD) is the source of ocular vascular dysfunction triggering GON. While some optic neuropathies are caused by hypoxia, the fluctuations in OBF triggering oxidative stress may contribute to glaucoma risk and progression. PVD commonly results in stiff and irregular retinal vessels, increased retinal venous pressure, impaired neuro-coupling, and decreased autoregulation capacity, all of which increase glaucoma risk and progression.
Evidence now exists that when vascular autoregulation is compromised, even normal BP and IOP fluctuation may lead to inconsistent OPP and subsequent ischemic ONH damage. For this reason, primary vascular dysregulation is a substantial risk factor for GON as it is associated with impaired autoregulation, low nocturnal BP, and increased retinal venous pressure – each of which can cause GON independently. It is reasonable to assume that reduced OBF from dysfunctional autoregulation may play a significant role in GON risk and progression. Furthermore, research findings suggest proper autoregulatory responses are altered or missing with glaucoma. These daily and repetitive ischemic events suggest a potential vascular mechanism in glaucoma, especially NTG. Despite this, vascular etiology in glaucoma is rarely considered amongst eye care professionals, even in NTG eyes with vasculopathic risk factors.
This evidence strongly suggests that elevated IOP alone does not cause GON, but rather diminished ocular blood flow, which is exacerbated by elevated IOP and reduced BP. While a vascular autoregulation system exists, PVD may limit or abolish this regulation capability leading to reduced OBF and subsequent ONH ischemic damage. Similarly, autoregulation capabilities may be exceeded in cases of elevated IOP, low BP, or OPP fluctuation. For these reasons, glaucoma progression is not resultant from high IOP or low BP alone, but in conjunction with decreased OPP resulting in ONH ischemia, axonal loss, and RGC death. This may explain why cardiovascular disease, hypertension, and diabetes are risk factors for glaucoma progression. Such evidence is biologically plausible and suggestive of a vasculopathic mechanism for progression.
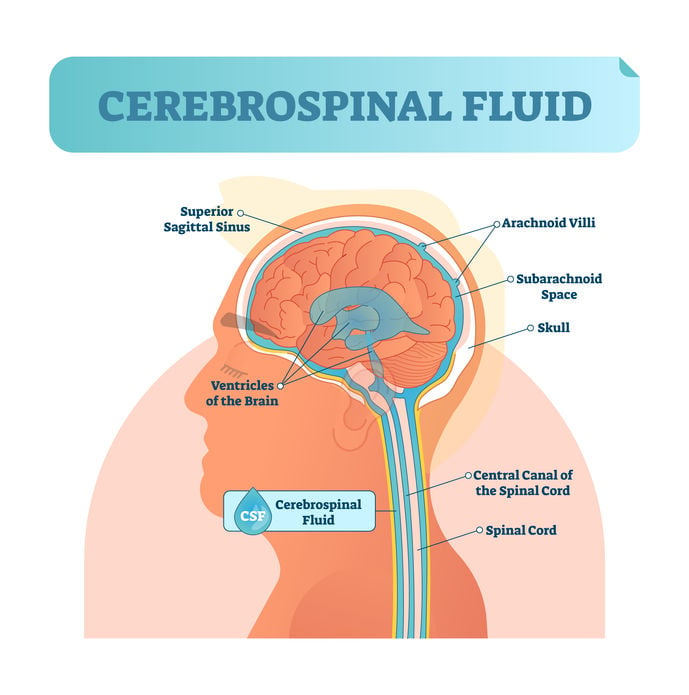
Während die Forschung weiter die Ansicht vertritt, dass verschiedene Arten von Druck eine Rolle bei GON spielen, deuten neue Ergebnisse darauf hin, dass ein bisher übersehener intrakranialer Druck existiert, der zum GON beitragen könnte. Interessanterweise deuten Studien bei Katzen darauf hin, dass ein Zusammenhang besteht zwischen einem niedrigen Liquordruck (engl. cerebrospinal fluid (CSF) pressure) und dem Entstehen eines Glaukoms. Damit in Zusammenhang steht, dass Personen mit einem Normaldruckglaukom (NTG) einen signifikant niedrigeren CSF-Druck aufweisen, als normale Probanden. Ähnliche Untersuchungen haben gezeigt, dass NTG-Probanden auch einen merklich schmaleren orbitalen zerebrospinalen Flüssigkeitsraum (ZSF-Raum) haben, der mit einem niedrigeren Liquordruck einhergeht, verglichen mit Glaukom-Probanden mit hohem IOD. Angesichts dessen, dass das Glaukom sich trotz eines normalen IOD entwickelt und fortschreitet, ist es plausibel, dass die Entstehung und die Progredienz des NTG sich teilweise aus einem niedrigen orbitalen Liquordruck ergibt, der mit einem engeren orbitalen zerebrospinalen Flüssigkeitsraum zusammenhängt. Die Untersuchungen sind noch nicht abgeschlossen, aber diese ersten Ergebnisse deuten darauf hin, dass der Druck hinter den Augen genauso signifikant ist, wie der Druck in den Augen, insbesondere bei NTG-Patienten.
.jpeg?width=500&name=Glaucoma%20Brain%20degeneration%20Restore%20Vision%20Clinic%20(1).jpeg)
Wie vorhin erwähnt, tritt, obwohl ein erhöhter IOD definitiv ein Risikofaktor für die Progredienz eines Glaukoms ist, eine Sehkraftverschlechterung oft auch dann auf, wenn der IOD mithilfe von medikamentösen und chirurgischen Behandlungen erfolgreich gesenkt wurde. Fälle wie diese legen einen IOD-unabhängigen Mechanismus nahe, der das Fortschreiten auslöst. Die Neuroimaging-Technologie hat das Potenzial, auf eine andere Seite des Glaukoms Licht zu werfen. Jahrzehntelang wurde das Glaukom von vielen Forschern und Ärzten als neurodegenerative Krankheit klassifiziert. Es bestehen Ähnlichkeiten zwischen dem Glaukom und neurogenerativen Erkrankungen, besonders der Parkinson- und Alzheimerkrankheit, was den Verlust von Neuronen, die transsynaptische Degeneration und den Zelltod betrifft. Jüngste Ergebnisse von Neuroimaging-Studien zeigen, dass Glaukom-Patienten fokale Hirnschäden in Bereichen außerhalb jenen der Netzhaut und des Sehnervs haben. Gehirntomographien bringen strukturale Veränderungen des seitlichen Kniehöckers (CGL), der Axone der Sehbahn (Tractus opticus) und der Sehrinde zum Vorschein, die mit einem Glaukom assoziiert werden.
Bemerkenswerterweise wurden strukturale Veränderungen selbst in nicht-visuellen Bereichen des Gehirns beobachtet. Neue faszinierende Beweise sind an den Tag gekommen, die zeigen, dass Glaukom-Patienten eine Atrophie der Amygdala erfahren, die potenziell zu Komplikationen bei Gefühlen und Gedächtnis führen können. Solche Anomalien der Amygdala könnten erklären, wieso Menschen, die an einem Glaukom leiden, oft Stimmungsschwankungen, vermehrte Angst, erhöhte Furchtsamkeit und Wutgefühle erleben.
Angesichts dieser neuen Entdeckungen könnte das Glaukom entweder eine primäre neurodegenerative Krankheit oder eine primäre optische Neuropathie mit sekundärer CNS-Schädigung sein. Vorausgesetzt, dass die Gesichtsfeldausfälle beim Glaukom eher mit den Nervenbündelfasermustern als mit den LGN-Verletzungen zu tun haben, ist das Glaukom vermutlich eine primäre optische Neuropathie mit sekundärer neurodegenerativer Beteiligung. Nichtsdestotrotz ist das Glaukom keine Krankheit des Auges alleine, sondern wird nun auch als Hirnerkrankung anerkannt.
Im Augenblick konzentrieren sich alle Behandlungsmodelle auf das Senken des IOD, was potenziell zu der Fehlinformation führen kann, das Glaukom würde nur durch einen hohen IOD verursacht werden. Lokal angewandte Medikamente, oral verabreichte Medikamente, die Laserchirurgie und Implantate, mit allen wird versucht, das Fortschreiten des Glaukoms durch die Reduktion des IOD zu beschränken. Es ist wohlbekannt, dass die Glaukom-Erkrankung bei manchen Patienten trotz niedrigem IOD fortschreitet, was einmal mehr darauf hindeutet, dass ein IOD-unabhängiger Mechanismus existiert.
Forschungsergebnisse deuten darauf hin, dass die vaskuläre Dysfunktion eine primäre Komponente bei Glaukom ist, und nicht sekundär auftritt. In Fällen einer systemischen Gefäßerkrankung sind die Blutgefäße steifer, irregulärer, zeigen reduzierte Neurokopplung und haben eine verminderte Autoregulationsfunktion. Anomalien wie diese sind nicht systemisch isoliert, sondern betreffen auch die Augen. Aufgrund der vaskulären Natur des Glaukoms ist es vernünftig, daraus zu schließen, dass das, was für das Gefäßsystem gesund ist, auch für die okulare Blutzufuhr gesund ist. Gefäßerkrankungsrisikofaktoren wie Bluthochdruck, Diabetes und Herz-Kreislauf-Erkrankungen zu reduzieren verringert vermutlich in ähnlicher Weise das Risiko für ein Glaukom und dessen Fortschreiten. Die Augenpflegedienstleister sollten auch besser mit den Hausärzten kommunizieren bezüglich der richtigen Anwendung blutdrucksenkender Medikamente, da ein merklicher Einfluss auf den OPP besteht und eine glaukomatösen Schädigung ausgelöst werden kann.
Das Glaukom ist vielleicht die fassettenreichste und am wenigsten verstandene Augenerkrankung angesichts der Tatsache, dass sowohl die Augen, die Gefäße als auch das Nervensystem involviert sind. Das Glaukom ist eine Sammlung progredienter optischer Neuropathien mit spezifischem Erscheinungsbild des ONH, dem Verlust von RGC-Axonen und Gesichtsfeldausfällen. Viel Verwirrung stammt daher, dass das Glaukom neurodegenerativ ist, eine vaskuläre Ätiologie hat und dennoch nur der IOD diskutiert und behandelt wird. Während der IOD ganz bestimmt ein Risikofaktor ist, hängt die Progredienz des Glaukoms vermutlich noch stärker mit der Ischämie durch einen verminderten okularen Perfusionsdruck zusammen, angesichts dessen, dass das Fortschreiten bei jeder Art von Blutdruck eintreten kann. Die Terminologie zum Glaukom, die Gedankenprozesse und die Behandlungen sind obsolet und führen zu einer unzureichenden Patientenschulung und schlechten Behandlungsergebnissen. In Zukunft werden die Glaukom-Mechanismen besser verstanden und verbesserte Behandlungsmethoden entwickelt werden, die die Entwicklung und das Fortschreiten des Glaukoms beschränken.
Blog ausgearbeitet in Kooperation mit Kaleb Abbott, O.D., M.S.

Hinweis: Die in diesem Blog veröffentlichte Informationen stellen die Ansichten des Autors dar und dienen nur der Weiterbildung des Lesers. Dieses Blog darf nicht als Ersatz für eine professionelle medizinische Beratung verstanden werden. Auch ersetzt oder beseitigt die geteilte Information keine offiziellen oder rechtlichen Begriffe für die Diagnose, Behandlung oder Pflege eines Glaukoms. Die Autoren übernehmen keinerlei Haftung für etwaige Unannehmlichkeiten oder Auswirkungen, die sich aufgrund der auf dieser Website geteilten Informationen ergeben.
REFERENCES
“Ich bin ausgesprochen zufrieden mit den Ergebnissen meiner Behandlung in der Restore Vision Clinic in Berlin. Ich habe ein Normaldruckglaukom und bekam laufend Medikament und wurde überwacht. Seit meiner Behandlung hat sich meine Nachtsicht verbessert und ich bekam eine andere Brille verschrieben. Ich brauche jetzt schwächere Gläser und mein Glaukom-Spezialist sagt, dass ich stabil zu sein scheine.“

Fedorov Restore Vision Clinic
Prenzlauer Allee 90
10409 Berlin (Germany)